Hóa học 10 Kết nối tri thức Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì được THPT Ngô Thì Nhậm biên soạn hy vọng sẽ là là tài liệu hữu ích giúp các em nắm vững kiến thức bài học và đạt kết quả tốt trong các bài thi, bài kiểm tra trên lớp.
Tóm tắt lý thuyết Hóa học 10 Kết nối tri thức Bài 7
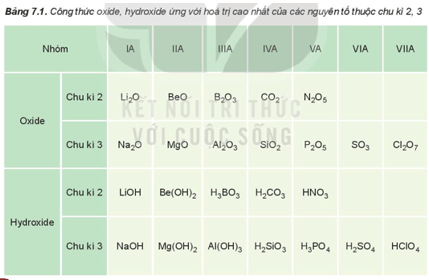
I. Thành phần của các oxide và hydroxide
– Hóa trị cao nhất của các nguyên tố nhóm A trong hợp chất với oxygen tăng từ I đến VII khi đi từ trái qua phải trong một chu kì (trừ chu kì 1 và nguyên tố fluorine ở chu kì 2), do đó thành phần của các oxide và hydroxide có sự lặp lại theo chu kì.
II. Tính chất của oxide và hydroxide
– Các oxide khi tác dụng với nước tạo thành hydroxide có tính base hoặc acid. Nói chung, hydroxide của các nguyên tố nhóm IA thể hiện tính base mạnh, hydroxide ứng với hóa trị cao nhất của các nguyên tố nhóm VIIA (trừ fluorine) thể hiện tính acid mạnh.
– Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, tính acid của chúng tăng dần.
Giải bài tập SGK Hóa học 10 Kết nối tri thức Bài 7
Câu hỏi 1 trang 40 Hóa học 10
Nguyên tố gallium thuộc nhóm IIIA và nguyên tố selenium thuộc nhóm VIA của bảng tuần hoàn. Viết công thức hóa học của oxide, hydroxide (ứng với hóa trị cao nhất) của hai nguyên tố trên.
Lời giải:
Nguyên tố gallium có công thức oxide và hydroxide lần lượt là Ga2O3 và Ga(OH)3.
Nguyên tố selenium có công thức oxide và hydroxide lần lượt là SeO3 và H2SeO4.
Câu hỏi 2 trang 42 Hóa học 10
Trong các chất dưới đây, chất nào có tính acid yếu nhất?
A. H2SO4.
B. HClO4.
C. H3PO4.
D. H2SiO3.
Lời giải:
Đáp án D
Các nguyên tố Si, P, S, Cl có điện tích tăng dần và cùng thuộc chu kì 3 nên tính acid của hydroxide ứng với hóa trị cao nhất tăng dần.
⇒ Acid H2SiO3 có tính acid yếu nhất.
Câu hỏi 3 trang 42 Hóa học 10
Dãy gồm các chất có tính base tăng dần là
A. Al(OH)3, Mg(OH)2, NaOH.
B. NaOH, Mg(OH)2, Al(OH)3.
C. Mg(OH)2, Al(OH)3, NaOH.
D. Al(OH)3, NaOH, Mg(OH)2.
Lời giải:
Đáp án A
Các nguyên tố Na, Mg, Al thuộc cùng chu kỳ, được xếp lần lượt theo chiều tăng của điện tích hạt nhân.
Lại có, trong một chu kì theo chiều tăng của điện tích hạt nhân tính base của oxide và hydroxide tương ứng giảm dần.
⇒ Dãy gồm các chất có tính base tăng dần là Al(OH)3, Mg(OH)2, NaOH.
Câu hỏi 4 trang 42 Hóa học 10
Những đại lượng và tính chất nào của nguyên tố hóa học cho dưới đây không biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử?
A. Tính kim loại và phi kim.
B. Tính acid – base của các hydroxide.
C. Khối lượng nguyên tử.
D. Cấu hình electron lớp ngoài cùng của nguyên tử.
Lời giải:
Đáp án C
Khối lượng nguyên tử không biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
Hoạt động 1 trang 41 Hóa học 10
Phản ứng của oxide với nước
Trong một thí nghiệm, cho lần lượt các oxide Na2O, MgO, P2O5 vào nước, nhúng giấy quỳ tím vào dung dịch sau phản ứng, hiện tượng phản ứng được trình bày trong bảng sau:
Oxide Hiện tượng Na2O Tan hoàn toàn trong nước.
Quỳ tím chuyển màu xanh đậm.
MgO Tan một phần trong nước.
Quỳ tím chuyển màu xanh nhạt.
P2O5 Tan hoàn toàn trong nước.
Quỳ tím chuyển màu đỏ.
1. Viết phương trình hóa học của các phản ứng xảy ra trong các thí nghiệm trên.
2. So sánh tính acid – base của các oxide và hydroxide tương ứng.
Lời giải:
1. Các phản ứng hóa học minh họa:
Na2O + H2O ⟶ 2NaOH
MgO + H2O ⟶ Mg(OH)2
P2O5 + 3H2O ⟶ 2H3PO4
2. Na2O; MgO là basic oxide; P2O5 là acidic oxide.
NaOH là base mạnh, Mg(OH)2 là base yếu, H3PO4 là acid trung bình.
Chiều giảm dần tính base và tăng dần tính acid của các oxide và hydroxide tương ứng:
Oxide: Na2O; MgO; P2O5
Hydroxide: NaOH; Mg(OH)2; H3PO4.
Hoạt động 2 trang 41 Hóa học 10
Phản ứng của muối với dung dịch acid
Chuẩn bị: dung dịch Na2CO3; dung dịch HNO3 loãng; ống nghiệm.
Tiến hành:
Thêm từng giọt dung dịch Na2CO3 vào ống nghiệm chứa dung dịch HNO3.
Quan sát hiện tượng và trả lời câu hỏi:
a) Viết phương trình hóa học của phản ứng.
b) Hãy so sánh độ mạnh, yếu giữa acid HNO3 và H2CO3.
Lời giải:
a) Phương trình hóa học của phản ứng:
Na2CO3 + 2HNO3 ⟶ 2NaNO3 + CO2↑ + H2O
b) Sau phản ứng H2CO3 sinh ra phân hủy ngay thành CO2 và H2O.
⇒ Acid HNO3 là acid mạnh và acid H2CO3 là acid yếu.
Em có thể trang 42 Hóa học 10
So sánh được tính acid và base của các oxide và hydroxide dựa vào vị trí nguyên tố tạo nên chúng trong bảng tuần hoàn nguyên tố hóa học.
Lời giải:
Để so sánh được tính acid và base của các oxide và hydroxide dựa vào vị trí nguyên tố tạo nên chúng trong bảng tuần hoàn nguyên tố hóa học cần ghi nhớ:
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
Trắc nghiệm Hóa 10 Kết nối tri thức Bài 7 (có đáp án)
Câu 1. Nguyên tố nào có công thức oxide (với hóa trị cao nhất) là R2O5?
A. Carbon (C);
B. Sodium (Na);
C. Sulfur (S);
D. Nitrogen (N).
Lời giải
Đáp án đúng là: D
Công thức oxide (với hóa trị cao nhất) là R2O5
R thuộc nhóm VA
Nguyên tố cần tìm là nitrogen (N).
Câu 2. Nguyên tố nào có công thức hydroxide (với hóa trị cao nhất) là R(OH)3?
A. Aluminium(Al);
B. Sodium (Na);
C. Sulfur (S);
D. Nitrogen (N).
Lời giải
Đáp án đúng là: A
Công thức hydroxide (với hóa trị cao nhất) là R(OH)3
R thuộc nhóm IIIA
Nguyên tố cần tìm là aluminium (Al).
Câu 3. Nguyên tử X có 17 proton. Hóa trị cao nhất của X trong hợp chất với oxygen là?
A. V;
B. VI;
C. VII;
D. VIII.
Lời giải
Đáp án đúng là: C
Nguyên tử X có 17 proton.
Cấu hình electron của X là: 1s22s22p63s23p5.
X thuộc nhóm VIIA.
Hóa trị cao nhất của X với oxygen là VII.
Câu 4. Nguyên tố X thuộc nhóm A của bảng tuần hoàn. Oxide ứng với hóa trị cao nhất của X là XO2. Số electron hóa trị của X là?
A. 3;
B. 4;
C. 5;
D. 6.
Lời giải
Đáp án đúng là: B
Oxide ứng với hóa trị cao nhất của X là XO2
X có hóa trị cao nhất trong hợp chất với oxygen là IV.
X có 4 electron hóa trị.
Câu 5. Nguyên tố X thuộc chu kì 3 nhóm VIIA. Công thức hóa học của hydroxide (ứng với hóa trị cao nhất) của X là?
A. H2XO3;
B. HX;
C. H2XO4;
D. HXO4.
Lời giải
Đáp án đúng là: D
Nguyên tố X thuộc chu kì 3 nhóm VIIA
X có 7 electron lớp ngoài cùng
Công thức hóa học của hydroxide (ứng với hóa trị cao nhất) của X là HXO4.
Câu 6. Nguyên tố X thuộc chu kì 3 nhóm VA. Cho các phát biểu sau:
(1) X là phosphorus
(2) Oxide ứng với hóa trị cao nhất là X2O7
(3) Hydroxide ứng với hóa trị cao nhất là H3XO4
(4) Hydroxide của X có tính base mạnh
Số các phát biểu đúng là?
A. 1;
B. 2;
C. 3;
D. 4.
Lời giải
Đáp án đúng là: B
Phát biểu đúng là: 1, 3.
(2) sai vì: Oxide ứng với hóa trị cao nhất là X2O5
(3) sai vì: Hydroxide của X có tính acid trung bình.
Câu 7. Phát biểu nào sau đây không đúng?
A. Hydroxide của các nguyên tố nhóm IA thể hiện tính base mạnh;
B. Hydroxide ứng với hóa trị cao nhất của các nguyên tố nhóm VIIA (trừ fluorine) thể hiện tính acid mạnh;
C. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng tăng dần;
D. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính acid của oxide và hydroxide tương ứng tăng dần.
Lời giải
Đáp án đúng là: C
C không đúng vì: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần.
Câu 8. Trong các acid sau, acid nào mạnh nhất?
A. HF;
B. HCl;
C. HBr;
D. HI
Lời giải
Đáp án đúng là: D
F, Cl, Br, I đều thuộc nhóm VIIA, tính acid tăng dần từ HF đến HI.
HI là acid mạnh nhất.
Câu 9. Trong các chất dưới đây, chất nào có tính base mạnh nhất?
A. Mg(OH)2;
B. NaOH;
C. Al(OH)3;
D. Fe(OH)3.
Lời giải
Đáp án đúng là: B
Trong các 4 hydroxide, chỉ có NaOH là hydroxide của kim loại nhóm IA nên NaOH có tính base mạnh nhất.
Câu 10. Trong các chất dưới đây, chất nào có tính acid mạnh nhất?
A. HClO4;
B. H2SiO3;
C. H3PO4;
D. H2SO4.
Lời giải
Đáp án đúng là: A
HClO4 là acid rất mạnh.
Câu 11. Dãy gồm các chất có tính base giảm dần là?
A. NaOH, Mg(OH)2, Al(OH)3;
B. NaOH, Al(OH)3, Mg(OH)2;
C. Mg(OH)2, Al(OH)3, NaOH;
D. Al(OH)3, Mg(OH)2, NaOH.
Lời giải
Đáp án đúng là: A
Dãy gồm các chất có tính base giảm dần là: NaOH, Mg(OH)2, Al(OH)3.
Giải thích:
Na, Mg, Al thuộc cùng một chu kì. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của hydroxide tương ứng giảm dần.
Câu 12. Dãy gồm các chất có tính acid tăng dần là?
A. H2SiO3, H3PO4, HClO4, H2SO4;
B. H2SO4, HClO4, H2SiO3, H3PO4;
C. H2SiO3, H3PO4, H2SO4, HClO4;
D. H2SO4, HClO4, H3PO4, H2SiO3.
Lời giải
Đáp án đúng là: C
Dãy gồm các chất có tính acid tăng dần là: H2SiO3, H3PO4, H2SO4, HClO4.
Giải thích:
Ta có Si, P, S, Cl thuộc cùng một chu kì.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính acid của các hydroxide tương ứng tăng dần.
Câu 13. Dãy gồm các chất có tính acid tăng dần là?
A. Al(OH)3; H2SiO3; H3PO4; H2SO4;
B. H2SiO3; Al(OH)3; Mg(OH)2; H2SO4;
C. NaOH; Al(OH)3; Mg(OH)2; H2SiO3;
D. H2SiO3; Al(OH)3; H3PO4; H2SO4.
Lời giải
Đáp án đúng là: A
Dãy gồm các chất có tính acid tăng dần là: Al(OH)3; H2SiO3; H3PO4; H2SO4.
Giải thích:
Ta có Al; Si; P; S thuộc cùng một chu kì.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính acid của các hydroxide tương ứng tăng dần.
Câu 14. Cho công thức oxide ứng với hóa trị cao nhất của X là XO3, trong đó X chiếm 40% về khối lượng. Xác định nguyên tố X.
A. Sulfur (S);
B. Phosphorus (P);
C. Carbon (C);
D. Nitrogen (N).
Lời giải
Đáp án đúng là: A
Công thức oxide ứng với hóa trị cao nhất của X là XO3, trong đó X chiếm 40% về khối lượng
MX/(MX+16×3)×100%=40%
Mx = 32
X là sulfur (S).
Câu 15. Cho công thức hydroxide ứng với hóa trị cao nhất của X là H3XO4, trong đó X chiếm 31,63% về khối lượng. Xác định nguyên tố X.
A. Sulfur (S);
B. Phosphorus (P);
C. Carbon (C);
D. Nitrogen (N).
Lời giải
Đáp án đúng là: B
Công thức hydroxide ứng với hóa trị cao nhất của X là H3XO4, trong đó X chiếm 31,63% về khối lượng
MX/(3+MX+16×4)×100%=31,63%
MX = 31
X là phosphorus (P).
******************
Trên đây là nội dung bài học Hóa học 10 Kết nối tri thức Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì do THPT Ngô Thì Nhậm biên soạn bao gồm phần lý thuyết, giải bài tập và các câu hỏi trắc nghiệm có đáp án đầy đủ. Hy vọng các em sẽ nắm vững kiến thức về Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì. Chúc các em học tập thật tốt và luôn đạt điểm cao trong các bài thi bài kiểm tra trên lớp.
Biên soạn bởi: Trường THPT Ngô Thì Nhậm
Chuyên mục: Hoá học 10